MAGELLAN-1
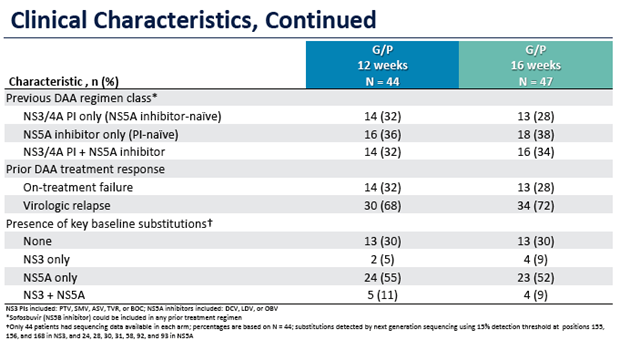
In MAGELLAN-1 wurden 91 Patienten (ca. 75% GT1a, 20% GT1b und 4% GT4; 30% Zirrhose) nach DAA-Versagen entweder 12 oder 16 Wochen mit Glecaprevir/Pibrentasvir (G/P) behandelt. Rund die Hälfte hatte nur NS5A-RAS,, 30% hatten keine RAS zu Baseline.
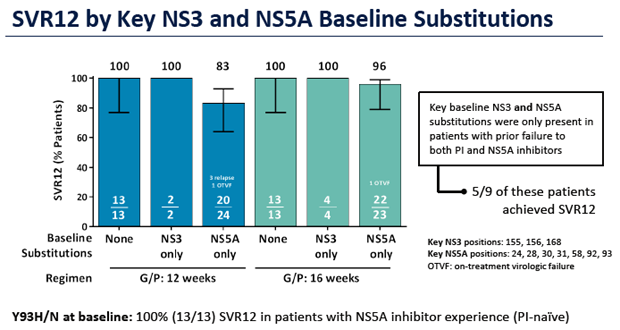
Es zeigte sich dass 12 Wochen
ausreichen bei Patienten ohne RAS und mit NS3-Resistenzmutationen
(SVR12 100%). Patienten mit NS5-RAS allein können mit 16 Woche G/P
geheilt werden (SVR12 96%). Lediglich bei Patienten mit NS3 – UND
NS5A-RAS scheint die Wirkung von G/P nicht ausreichend zu sein. Von
neun Patienten mit dieser Konstellation erreichten vier die SVR12.
HCV-Heilung macht Lebertransplantation überflüssig
Jeder vierte geheilte Patient konnte von der Warteliste genommen werden.
In einer italienischen retrospektiven Analyse wurden die Daten von 142 Patienten mit Hepatitis C und dekompensierter Zirrhose (ohne HCC) ausgewertet, die zwischen 2/2014 und 6/2015 für eine Lebertransplantation gelistet wurden.
Nach DAA-Therapie konnten 38/142 (24%) der Patienten von der Warteliste genommen werden. Der mittlere MELD – bzw. CP-Score war vor Therapie 14 bzw. 9 und verbesserte sich auf 9 bzw. 6. Die mittlere Beobachtungszeit seit DAA-Therapie betrug 28 Monate, seit Delisting 15 Monate. Nur ein Patient verschlechterte sich so, dass er wieder gelistet wurde.