2D/3D-Regime im deutschen HEP-C-Register
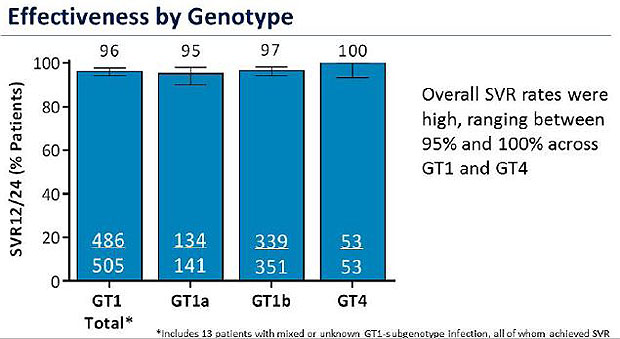
Ausgewertet wurden die Daten von 1071 Patienten mit GT1/4, die mit 2D/3D mit/ohne Ribavirin behandelt wurden. 60% der Patienten waren vorbehandelt, 12% davon mit einer Boceprevir/Telaprevir-basierten Tripletherapie. 60% hatten GT1b, 26% GT1a, 12% GT4. 22% hatten eine Zirrhose, 7% eine dekopmensoierte Zirrhose. 60% hatten eins oder mehrere zusätzliche Medikamente.
Die SVR-Raten lagen zwischen 95% (GT1a) und 100% (GT4). Alle 9 Patienten mit einer GRF <30 ml/Min ereichten die SVR12.
Nur 1,1% der Patienten erlitten einen Relaps (6/558). Prädiktoren waren nicht nachzuweisen. 3/6 waren mit einem Proteasehemmer vorbehandelt; 1/6 hatte eine Zirrhose; 2/6 waren nicht gemäß den Leitlinien behandelt worden.
Die Verträglichkeit war sehr gut,
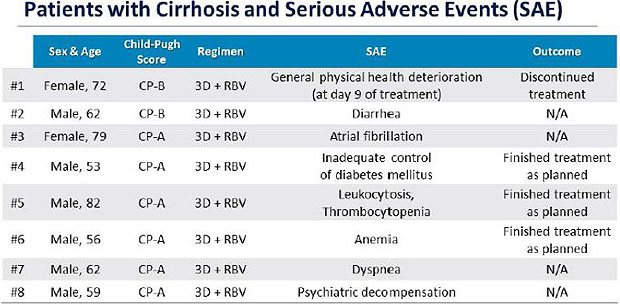
insbesondere ohne Ribavirin. 9 Patienten mit Zirrhose mussten die
Therapie wegen Nebenwirkungen abbrechen und bei 8 Patienten mit
Zirrhose wurde ein SAE dokumentiert, was jedoch nur bei einem
Patienten zum Abbruch führte.