Kommentar Prof. Dr. Thomas Berg, Leipzig
Antikörper gegen HBs und ein HBsAg-Verlust sind in der Regel ein Zeichen dafür, dass die Hepatitis B abgeheilt ist.
Doch was,
wenn trotz anti-HBs bzw. HBs-Verlust noch Viren vorhanden sind?
 Prof. Dr. med. Thomas Berg
Prof. Dr. med. Thomas BergKlinik und Poliklinik für
Gastroenterologie
Sektion Hepatologie
Universitätsklinikum Leipzig
Liebigstr. 20 · 04103 Leipzig
E-Mail: thomas.berg@
medizin.uni-leipzig.de
Fall 1
beschreibt eine Patientin mit einer chronischen HBeAg positiven Hepatitis B mit gering erhöhten Transaminasen und moderater Virämie. Wahrscheinlich liegt ein gering-aktive chronische Hepatitis B vor.
Die Transmission erfolgte bei der jungen Vietnamesin, deren Mutter auch an einer HBV Infektion leidet, mit hoher Wahrscheinlichkeit während der Geburt (vertikale Transmission). In diesen Fällen entwickelt sich initial meist eine HBeAg positive chronische HBV Infektion (sogenannte „immuntolerate“ HBV Infektion), die im Erwachsenenalter dann oft in eine „immunaktive“ chronische HBeAg-positive Hepatitis übergeht.
Ein chronischer Verlauf muss angenommen werden, da bereits vor 5 Jahren eine HBV Infektion diagnostiziert worden war. Würde diese Information nicht vorliegen, wäre auch eine akute Infektion denkbar, mit jetzt rückläufigen Transaminasen und möglicherweise beginnender Serokonversion. Es wäre interessant zu wissen, ob die Patientin bereits anti-HBe-Antikörper entwickelt hat, die auch gleichzeitig beim Nachweis von HBeAg bei Patienten mit beginnender HBeAg-Serokonversion vorliegen können.
Das HBsAg ist der erste HBV-Seromarker, der bei einer HBV Neuinfektion ca. 2-10 Wochen nach der HBV-Exposition nachgewiesen werden kann. Bei Personen mit selbstlimitierender Infektion verschwindet das HBsAg innerhalb von 4-6 Monaten, meist assoziiert mit dem Auftreten von anti-HBs Antikörpern. Das Erscheinen der anti-HBs Antikörper zeigt somit in aller Regel die Ausheilung der HBV Infektion und Entwicklung einer HBV Immunität an.
Die Koexistenz von HBsAg und anti-HBs ist eine ungewöhnliche serologische Konstellation in der klinischen Praxis, die jedoch bereits seit 1976 bekannt ist (1; Arnold et al. 1976). Inzwischen existieren weltweit zahlreiche große epidemiologische Studien, die die Koexistenz von anti-HBs bei HBsAg-positiven Patienten in einer Frequenz von ca. 2-10% beschreiben.2-6 Mutationen im HBV Genom, die eine Selektion von HBsAg „immune-escape“ Varianten ermöglichen, konnten in der Mehrzahl der Fälle mit Koexistenz von HBsAg und anti-HBs nachgewiesen werden.3,6-10 Von besonderer Relevanz sind hierbei vor allem HBV „escape“ Mutanten innerhalb der S Region (major hydrophilic region) sowie Deletionsmutationen in the pre-S Region.7, 11 Neben Änderungen der Struktur und Antigenität des HBsAg durch Mutationen im HBV S-Gen können auch andere Ursachen für die Koexistenz verantwortlich sein:
1.Eine anti-HBs Subtyp Unspezifität zum Beispiel durch eine HBV Superinfektion mit einem neuen (zweiten) HBV Serotyp und somit einer „falschen“ unspezifischen anti-HBs Response gegenüber dem nicht-homologen HBsAg der Erstinfektion.
2. Eine HBV-Reaktivierung unter Immunsuppression und
3. kann auch ein falsch positiver Anti-HBs-Test nicht ausgeschlossen werden.7, 12
Die klinische Bedeutung der Koexistenz von HBsAg und anti-HBs ist nicht eindeutig geklärt. Eine höhere Prävalenz von anti-HBs Antikörpern konnte jedoch bei Patienten mit aktiver chronischer Hepatitis B im Vergleich zu inaktiven HBsAg-Trägern nachgewiesen werden13, und die Persistenz von anti-HBs war mit einem höheren Risiko für die Entwicklung einer fortgeschrittenen Fibrose und eines HCC assoziiert.3,5,13,14
Procedere: Im Fall 1 sollte die HBeAg, anti-HBe und anti-HBs Konzentrationen und die HBV DNA nochmals nach 3 Monaten bestimmt werden. Ist es nicht zu einer HBeAg-Serokonversion gekommen und bestätigt sich die HBeAg-positive chronische Hepatitis B und so ist unabhängig von der anti-HBs Konzentration eine antivirale Therapie indiziert, da einiges dafür spricht, dass die chronische Hepatitis B bei Koexistenz von anti-HBs ein höheres Krankheitsprogressionsrisiko besitzt.
Fall 2
beschreibt eine junge Patientin, die offenbar im Rahmen ihres Drogenkonsums im September 2015 eine akute HBV Infektion erlitten hat mit chronischem Verlauf. Ein Jahr später wurde bei Nachweis einer deutlichen Hepatitisaktivität mit 5-fach erhöhten ALT Werten und hoher Virämie eine antivirale Therapie mit Tenofovir begonnen. Der HBeAg Status ist nicht dokumentiert. Zwei Jahre nach Therapiebeginn und unter regelmäßiger Medikamenteneinnahme ist es zu einem Verlust von HBsAg gekommen, jedoch lässt sich trotz Negativität für HBsAg eine geringe Hepatitis B Virämie nachweisen. Anti-HBs Konzentrationen wurden nicht bestimmt.
Der anhaltende Nachweis von HBV-Genom in der Leber mit oder ohne Nachweis von HBV-DNA im Serum bei HBsAg-negativen Personen wird als okkulte HBV Infektion bezeichnet.15-17 Anhand der serologischen Konstellation ist es möglich, verschiedene Varianten der OBI voneinander zu unterscheiden (siehe Abb.). Die Ursachen der fehlenden HBsAg Produktion trotz Nachweis Replikations-kompetenten HBV-Genoms sind im Detail nicht gut verstanden, aber es gibt Hinweise, dass sowohl immunologische als auch virologische Faktoren eine Rolle spielen. Bestimmte virale S-Antigen Mutationen können sowohl zu einer verminderten Sekretion viraler Partikel führen, als auch zu einer verminderten Bindungsaffinität gegenüber den in kommerziellen Tests verwendeten anti-HBs-Antikörpern.18,19 Auch die Sensitivität der HBsAg Tests kann für den fehlenden Nachweis von HBsAg verantwortlich sein. Mittels hochsensitiver HBsAg-Tests (Luminpulse HBsAg-HQ, Fujirebio), der im Vergleich zu den bisherigen Tests eine ca. 10-fach höhere Sensitivität besitzt, können in bis zu 30% aller OBI-Fälle niedrige HBsAg Konzentration nachgewiesen werden.20,21 Eine Vorbehandlung der Proben zum Lösen von Immunkomplexen erhöht die Rate positiver HBsAg Nachweise zusätzlich, so dass HBsAg-anti-HBs Immunkomplexe auch eine Ursache für den fehlenden HBsAg Nachweis bei OBI-Patienten darstellen können.22
Klinische
Relevanz hat die OBI vor allem in der Transfusionsmedizin.
HBV-Übertragungen durch Blut- und Blutprodukte
HBsAg-negativer
aber HBV-DNA-positiver Spender waren der Grund ein generelles HBV-DNA
Screening einzuführen. Reaktivierungen der OBI mit Entwicklung einer
fulminanten Hepatitis sind unter immunsuppressiver Therapie gut
dokumentiert. Darüber hinaus scheint die OBI vor allem bei Patienten
mit chronischen Lebererkrankungen (z.B. chronische Hepatitis C) einen
signifikanten Risikofaktor für die Fibroseprogression und
HCC-Entwicklung darzustellen (siehe Übersicht 15,
17).
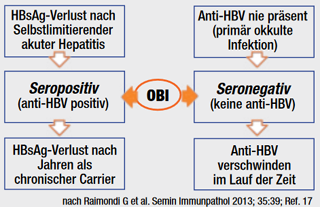
Abb. Schematische Darstellung der verschie- denen Konstellationen, die zu unterschiedlichen serologischen Profilen einer okkulten HBV-In- fektion (OBI) führen können
Procedere: Im Fall 2 zeigt sich jetzt ca. 2 Jahre nach antiviraler Therapie ein HBsAg-Verlust mit Nachweis von anti-HBs in einer Konzentration von 110 IU/ml. Trotz fehlendem Nachweis von HBsAg ist die HBV DNA gering erhöht im Serum nachweisbar. Es liegt also aktuell eine okkulte HBV Infektion (OBI) vor. Zusätzlich besteht ein Zustand nach HCV Infektion (offenbar spontane Elimination). Der Befund gering nachweisbarer HBV-DNA bei Verlust von HBs Ag und Bildung von anti-HBs ist im Rahmen der Therapie-induzierten Elimination als transientes Phänomen vorstellbar (Abb.).
Es wäre zu empfehlen die Parameter nochmals zu kontrollieren. Es ist nicht unwahrscheinlich, dass im weiteren Verlauf die HBV DNA negativ getestet wird. Ich würde dann aufgrund der erfolgten Serokonversion noch eine Konsolidierungstherapie über 6-12 Monate durchführen; dann kann die Therapie beendet werden. Selbst bei gering erhöhten HBV-DNA Konzentrationen wäre bei bestätigter HBsAg-Serokonversion ein Auslassversuch gerechtfertigt unter engmaschiger Kontrolle von HBsAg quantitativ, anti-HBs, HBV DNA und Transaminasen.
1 Arnold W, Hess G, Meyer ZBK et al: Simultaneous occurrence in the serum of hepatitis B surface antigen (HBsAg) and antibodies against HBsAg (Anti- HBs) of different subtypes. (Serologic and fluorescence histologic studies). Verh Dtsch Ges Inn Med, 1976; 82: 405-7.
2 Ding F, Yu HG, Li YX, Cui N, Dai JF, Yu JP. Sequence analysis of the HBV S protein in Chinese patients with coexisting HBsAg and anti-HBs antibodies. J Med Virol. 2015; 87: 2067-2073.
3 Seo SI, Choi HS, Choi BY, Kim HS, Kim HY, Jang MK. Coexistence of hepatitis B surface antigen and antibody to hepatitis B surface may increase the risk of hepatocellular carcinoma in chronic hepatitis B virus infection: a retrospective cohort study. J Med Virol. 2014; 86: 124-130.
4 Colson P, Borentain P, Motte A, Henry M, Moal V, Botta-Fridlund D, et al. Clinical and virological significance of the co-existence of HBsAg and anti-HBs antibodies in hepatitis B chronic carriers. Virology 2007; 367: 30-40.
5 Lee BS, Cho YK, Jeong SH, Lee JH, Lee D, Park NH, et al. Nationwide seroepidemiology of hepatitis B virus infection in South Korea in 2009 emphasizes the coexistence of HBsAg and anti-HBs. J Med Virol. 2013; 85: 1327-1333.
6 Lada O, Benhamou Y, Poynard T, Thibault V. Coexistence of hepatitis B surface antigen (HBs Ag) and anti-HBs antibodies in chronic hepatitis B virus carriers: influence of „a“ determinant variants. J Virol. 2006; 80: 2968-2975.
7 Pondé RA. The underlying mechanisms for the „simultaneous HBsAg and anti-HBs serological profile“. Eur J Clin Microbiol Infect Dis. 2011; 30: 1325-1340.
8 Liu W, Hu T, Wang X, Chen Y, Huang M, Yuan C, et al. Coexistence of hepatitis B surface antigen and anti-HBs in Chinese chronic hepatitis B virus patients relating to genotype C and mutations in the S and P gene reverse transcriptase region. Arch Virol. 2012; 157: 627-634.
9 Chen Y, Qian F, Yuan Q, Li X, Wu W, Guo X, et al. Mutations in hepatitis B virus DNA from patients with coexisting HBsAg and anti-HBs. J Clin Virol. 2011; 52: 198-203.
10 Gerlich WH. The enigma of concurrent hepatitis B surface antigen (HBsAg) and antibodies to HBsAg. Clin Infect Dis. 2007; 44: 1170-1172.
11 Huang X, Qin Y, Zhang P et al: PreS deletion mutations of hepatitis B virus in chronically infected patients with simultaneous seropositivity for hepatitis-B surface antigen and anti-HBS antibodies. J Med Virol, 2010; 82(1): 23-31.
12 Fu X, Chen J, Chen H, Lin J, Xun Z, Li S, Liu C, Zeng Y, Chen T, Yang B, Ou Q. Mutation in the S gene of hepatitis B virus and anti-HBs subtype-nonspecificity contributed to the co-existence of HBsAg and anti-HBs in patients with chronic hepatitis B virus infection. J Med Virol. 2017 Aug;89(8):1419-1426.
13 Shiels MT, Taswell HF, Czaja AJ et al: Frequency and significance of concurrent hepatitis B surface antigen and antibody in acute and chronic hepatitis B. Gastroenterology, 1987; 93(4): 675-80.
14 Jang JS, Kim HS, Kim HJ et al: Association of concurrent hepatitis B surface antigen and antibody to hepatitis B surface antigen with hepatocellular carcinoma in chronic hepatitis B virus infection. J Med Virol, 2009; 81(9): 1531-38.
15 Raimondo G, Allain JP, Brunetto MR, Buendia MA, Chen DS, ColomboM, Craxi A, Donato F, Ferrari C, Gaeta GB, GerlichWH, LevreroM, Locarnini S, Michalak T, Mondelli MU, Pawlotsky JM, Pollicino T, Prati D, Puoti M, Samuel D, Shouval D, Smedile A, Squadrito G, Trepo C, Villa E,Will H, Zanetti AR, Zoulim F. Statements from the Taormina expert meeting on occult hepatitis B virus infection. J Hepatol 2008; 49:652-657.
16 Cacciola I, Pollicino T, Squadrito G, Cerenzia G, Orlando ME, Raimondo G. Occult hepatitis B virus infection in patients with chronic hepatitis C liver disease. N Engl J Med 1999; 341:22-26.
17 Raimondi G, Caccamo G, Filomia R, Pollicino T. Occult HBV infection. Semin Immunpathol 2013; 35:39.
18 Xiang KH, Michailidis E, Ding H, Peng YQ, Su MZ, Li Y, Liu XE, Dao Thi VL, Wu XF, Schneider WM, Rice CM, Zhuang H, Li T. Effects of amino acid substitutions in hepatitis B virus surface protein on virion secretion, antigenicity, HBsAg and viral DNA. J Hepatol. 2017; 66: 288-296.
19 Zhang K, Liu Y, Chen R, Li Q, Xu Z, Si L, Cheng Y, Yang Y, Chen J, Xu D, Lin S. Antigenicity reduction contributes mostly to poor detectability of HBsAg by hepatitis B virus (HBV) S-gene mutants isolated from individuals with occult HBV infection. J Med Virol. 2018; 90: 263-270.
20 Shinkai N, Kusumoto S, Murakami S, Ogawa S, Ri M, Matsui T, Tamori A, Toyoda H, Ishida T, Iida S, Tanaka Y. Novel monitoring of hepatitis B reactivation based on ultra-high sensitive hepatitis B surface antigen assay. Liver Int. 2017; 37: 1138-1147.
21 Deguchi M, Kagita M, Yoshioka N, Tsukamoto H, Takao M, Tahara K, Maeda I, Hidaka Y, Yamauchi S, Kaneko A, Miyakoshi H, Isomura M. Evaluation of the highly sensitive chemiluminescent enzyme immunoassay „Lumipulse HBsAg-HQ“ for hepatitis B virus screening. J Clin Lab Anal. 2018; 32: e22334.
22 Matsumoto A, Imaizumi M, Tanaka Y, Nishiguchi S, Yatsuhashi H, Ishida T, Moriyama K, Aoyagi K, Tanaka E. Novel and highly sensitive immunoassay for total hepatitis B surface antigen, including that complexed with hepatitis B surface antibody. J Gastroenterol. 2017; 52: 376-384.